近日,国务院印发《关于深化“证照分离”改革进一步激发市场主体发展活力的通知》(以下简称《通知》)。《通知》强调,自2021年7月1日起,在全国范围内实施涉企经营许可事项全覆盖清单管理,按照直接取消审批、审批改为备案、实行告知承诺、优化审批服务等四种方式分类推进审批制度改革。
据查询发现,在《通知》中,涉及卫健、药监部门的改革项目有67项之多。其中,多项政策针对放宽对社会办医和诊所审批的限制,包括“开办诊所不再向卫生健康部门申请办理设置审批,直接办理诊所执业备案”、三级以外医疗机构取消“设置医疗机构审批书”、诊所执业由许可管理改为备案管理等。

简政放权!7月1日起迎大改革
本次“证照分离”改革,实际上是在2018年全国推开“证照分离”改革的基础上的“深化”。
改革要求是持续深化“放管服”改革,统筹推进行政审批制度改革和商事制度改革,在更大范围和更多行业推动照后减证和简化审批,创新和加强事中事后监管,进一步优化营商环境、激发市场主体发展活力,加快构建以国内大循环为主体、国内国际双循环相互促进的新发展格局。
改革目标是自2021年7月1日起,在全国范围内实施涉企经营许可事项全覆盖清单管理,清单分3类,第一类是中央层面设定的许可事项改革清单(2021年全国版)共523项,第二类是中央层面设定的许可事项改革清单(2021年自由贸易试验区版)共69项。第三类是国务院决定在自由贸易试验区暂时调整适用行政法规有关规定目录。
按照直接取消审批、审批改为备案、实行告知承诺、优化审批服务等四种方式分类推进审批制度改革,同时在自由贸易试验区进一步加大改革试点力度,力争2022年底前建立简约高效、公正透明、宽进严管的行业准营规则,大幅提高市场主体办事的便利度和可预期性。
初略统计,本次“证照分离”改革共涉及医疗卫生事项31项,在“全国版”中涉及医疗卫生行业的事项共计24项。其中直接取消审批5项、审批改为备案1项、实行告知承诺2项、优化审批服务16项。在“自由贸易试验区版”中涉医事项4项,其中审批改备案2项,实行告知事项2项。国务院决定在自由贸易试验区暂时调整适用行政法规涉医法规3个。
诊所设置审批取消了!
5项取消的审批包括诊所设置审批、计划生育技术服务机构执业许可证、设置医疗机构批准书、职业卫生技术服务机构资格甲级证书、职业卫生技术服务机构资格丙级证书。
重点说与社会办医关系密切的诊所设置审批和设置医疗机构批准书两项。
按照《医疗机构管理条例》,县级以上地方人民政府卫生行政部门应当根据本行政区域的人口、医疗资源、医疗需求和现有医疗机构的分布状况,制定本行政区域医疗机构设置规划。单位或者个人设置医疗机构,必须经县级以上地方人民政府卫生行政部门审查批准,并取得设置医疗机构批准书。
因此,之前依《条例》规定,设置诊所等医疗机构首先必须符合规划并取得《设置医疗机构批准书》,然后才能按照《设置医疗机构批准书》载明的事项进行建设,包括选址、规模、设备购置安装等,待建设完成后,再申请批准设置的部门组织现场验收,达标后才会进行医疗机构执业登记,发给《医疗机构执业许可证》方可开门营业。
2016年2月6日国务院第666号令对条例进行了修改,明确机关、企业和事业单位按照国家医疗机构基本标准设置为内部职工服务的门诊部、诊所、卫生所(室),报所在地的县级人民政府卫生行政部门备案。但并没有放开面向社会提供服务的诊所实行备案管理。
2017年2月28日,国家卫生计生委第13号令发布了《医师执业注册管理办法》并决定在4月1日正式实施,这一改革最大的亮点就是确立了医师区域注册制度,将医师执业地点由过去的“医疗、预防、保健机构”修改为“医疗、预防、保健机构所在地的省级或者县级行政区划”。
2018年6月,关于进一步改革完善医疗机构、医师审批工作的通知规定,6月底前,全国全面实施电子化注册管理。同年10月,国务院关于在全国推开“证照分离”改革的通知(国发〔2018〕35号)对医疗机构执业登记和医师执业注册两项进行了改革,但主要内容是推广网上办理,加快电子化注册,压缩审批时限,精简审批材料,逐步实现社会办营利性医疗机构床位数由投资主体自主决定等。
2019年4月28日,国家卫健委等五部委联合印发开展促进诊所发展试点意见的通知(国卫医发〔2019〕39号)首次在国家级正式文件中提出,将诊所设置审批改为备案制管理,举办诊所的,报所在地县(区)级卫生健康行政部门备案,发放《医疗机构执业许可证》后,即可开展执业活动。跨行政区域经营的连锁化、集团化诊所由上一级卫生健康行政部门统一备案,跨省级行政区域经营的由所在省份卫生健康行政部门分别备案。但仅在北京、上海、沈阳、南京、杭州、武汉、广州、深圳、成都、西安等10个城市试点。
这一次,国务院《通知》提出直接取消诊所设置审批和设置医疗机构批准书两项,显然是要在全国所有地区执行。其中取消诊所设置审批是指开办诊所不再向卫生健康行政部门申请办理设置审批,直接办理设置备案,取得设置备案书即可开业。
取消《设置医疗机构批准书》是指除三级医院、三级妇幼保健院、急救中心、急救站、临床检验中心、中外合资合作医疗机构、港澳台独资医疗机构外,举办其他医疗机构的,卫生健康行政部门不再核发《设置医疗机构批准书》,仅在执业登记时发放《医疗机构执业许可证》。这实际上与2018年国卫医发〔2018〕19号《关于进一步改革完善医疗机构、医师审批工作的通知》要求一致。
社会办医乙类大型医用设备配置大放开
审批改为备案3项,包括诊所执业登记、社会办医疗机构乙类大型医用设备配置许可、公共场所卫生许可证3项。关于诊所亦如前述,这里不再赘述。
这里主要谈谈社会办医疗机构乙类大型医用设备配置许可。
2018年5月,国家卫健委和国家药监局联合印发的大型医用设备配置与使用管理办法(试行)规定,大型医用设备目录由国家卫生健康委员会商国务院有关部门提出,报国务院批准后公布执行。国家按照目录对大型医用设备实行分级分类配置规划和配置许可证管理。
大型医用设备配置管理目录分为甲、乙两类。甲类大型医用设备由国家卫生健康委员会负责配置管理并核发配置许可证;乙类大型医用设备由省级卫生健康行政部门负责配置管理并核发配置许可证。违反规定,超规划、越权或违法实施大型医用设备配置许可的,依据《行政许可法》、《医疗器械监督管理条例》等有关规定予以处理。这就是说,不管谁出钱,没有配置许可,没有省级卫生健康行政部门批准任何医疗机构均不得配置乙类大型设备。
目前乙类医疗设备包括:1.X线电子计算机断层扫描装置(CT)。2.医用核磁共振成像设备(MRI)。3.数字减影血管造影X线机(DSA)。4.医用电子直线加速器(LA)。5.单光子发射型电子计算机断层扫描装置(SPECT)。
2018年1月17日国务院常务会议决定,在上海浦东新区,将取消社会办医疗机构乙类大型医用设备配置许可证核发等审批。随后,国务院正式公布《关于在上海市浦东新区暂时调整实施有关行政法规规定的决定》(国发〔2018〕29号),决定即日起至2018年12月31日,在上海市浦东新区暂时调整实施《医疗器械监督管理条例》第三十四条第二款关于大型医用设备配置许可证核发的规定,对试点区域内的社会办医疗机构配置乙类大型医用设备不实行许可管理。
这是对于上海浦东新区的临时性政策。
自2013年9月上海第一个自由贸易试验区设立以来,至2020年9月我国在20多个省设立了自由贸易试验区。因此,这次《通知》决定在自由贸易试验区取消社会办医机构乙类医用设备配置许可管理改为备案管理,尽管没有决定在全国实行,但实际上也是将上海自贸区试行的这一政策在更大范围推广,必将惠及更多自贸区的医疗机构。
此外,还实行告知承诺4项,包括公共场所卫生许可证社会办医疗机构乙类大型设备配置许可证、消毒产品生产企业许可证、麻醉药品和第一类精神药品购用印鉴卡4项。
优化审批服务16项,主要包括饮用水单位卫生许可证、生产用于传染病防治的消毒产品的单位审批、放射卫生技术服务机构资质证书、放射诊疗许可证、医疗机构执业许可证(从事戒毒服务)、人类辅助生殖技术许可批件、母婴保健技术服务许可证、器官移植诊疗科目登记、医疗机构设置批准书(指还需要的医疗机构)、医疗机构(不含诊所)执业登记、职业技术服务机构乙级资质许可、血站的设立即执业登记、单采血浆站设置审批即许可证核发、人类精子库批准证书、麻醉药品即第一类精神药品购用印鉴卡、社会办医疗机构甲类大型设备配置许可。
自贸区政策优惠力度更大
一是《放射性药品管理办法》。办法第二十一条规定,医疗单位使用放射性药品,必须符合国家有关放射性同位素安全和防护的规定。所在地的省、自治区、直辖市药品监督管理部门,应当根据医疗单位核医疗技术人员的水平、设备条件,核发相应等级的《放射性药品使用许可证》,无许可证的医疗单位不得临床使用放射性药品。
第二十三条规定,持有《放射性药品使用许可证》的医疗单位,必须负责对使用的放射性药品进行临床质量检验,收集药品不良反应等项工作,并定期向所在地药品监督管理、卫生行政部门报告。由省、自治区、直辖市药品监督管理、卫生行政部门汇总后分别报国务院药品监督管理、卫生行政部门。本次《通知》明确医疗单位使用放射性药品(一二类)直接取消。
二是医疗器械监督管理条例。条例第三十四条规定,医疗器械使用单位配置大型医用设备,应当符合国务院卫生计生主管部门制定的大型医用设备配置规划,与其功能定位、临床服务需求相适应,具有相应的技术条件、配套设施和具备相应资质、能力的专业技术人员,并经省级以上人民政府卫生计生主管部门批准,取得大型医用设备配置许可证。
第六十三条规定,未经许可擅自配置使用大型医用设备的,由县级以上人民政府卫生计生主管部门责令停止使用,给予警告,没收违法所得;违法所得不足1万元的,并处1万元以上5万元以下罚款;违法所得1万元以上的,并处违法所得5倍以上10倍以下罚款;情节严重的,5年内不受理相关责任人及单位提出的大型医用设备配置许可申请。由于《通知》已经明确自贸区内社会办医疗机构购置乙类大型设备已经由审批改为备案,因此在条例中这两条相应暂时做调整。
三是公共场所卫生管理条例。该条例规定,国家对公共场所实行“卫生许可证”制度。本《通知》调整决定将“音乐厅;展览馆、博物馆、美术馆、图书馆;书店、录像厅(室)”这几类场所的公共卫生许可审批改为备案。
放管服之后,监管也要加强了!
近年来,各级政府积极推进放管服改革,很多地方都设立了统一的行政审批部门,实行集中审批。但却存在着审批与监管脱节现象,本次《通知》明确要求适应改革要求明确监管责任。提出要落实放管结合、并重要求,按照“谁审批、谁监管,谁主管、谁监管”原则,切实履行监管职责,坚决纠正“以批代管”、“不批不管”问题,防止出现监管真空。
直接取消审批、审批改为备案的,由原审批部门依法承担监管职责。实行告知承诺、优化审批服务的,由审批部门负责依法监管持证经营企业、查处无证经营行为。实行相对集中行政许可权改革或者综合行政执法改革的地区,按照省级人民政府制定的改革方案确定监管职责、健全审管衔接机制。
对直接涉及公共安全和人民群众生命健康等特殊行业、重点领域,落实全覆盖重点监管,强化全过程质量管理,守牢安全底线。
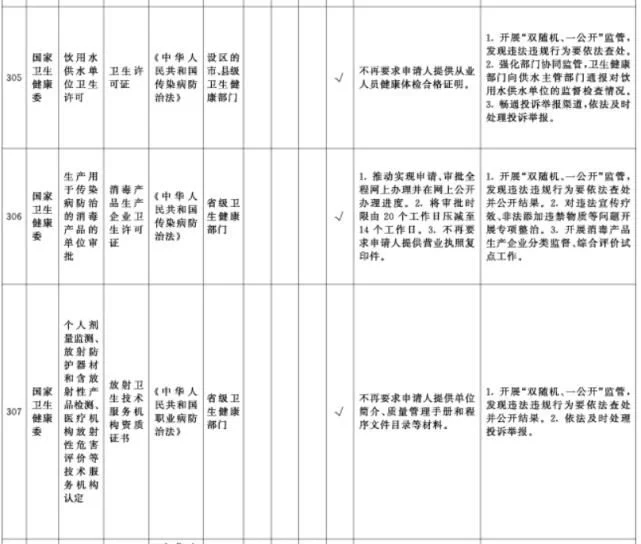
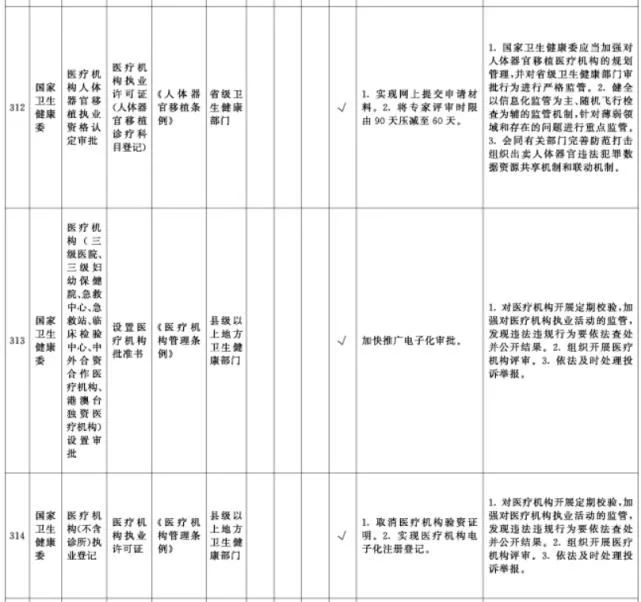
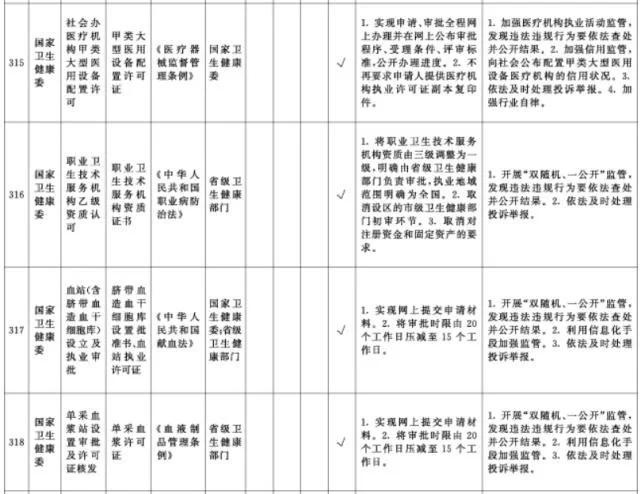
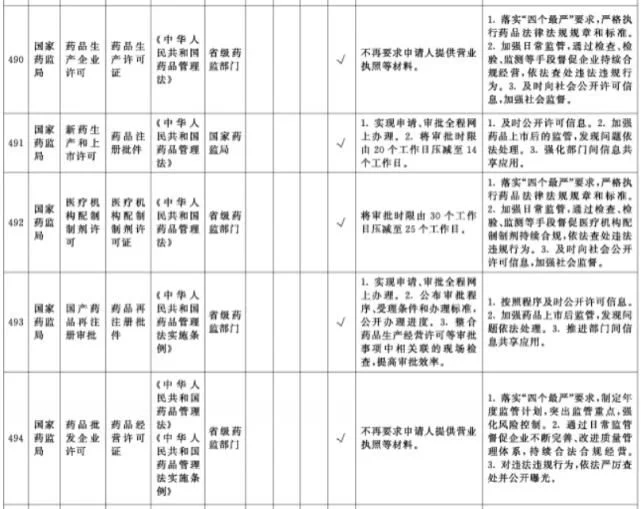
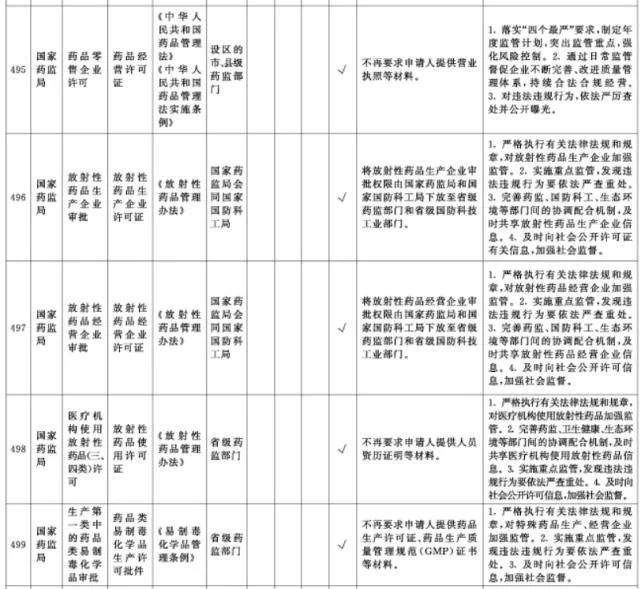
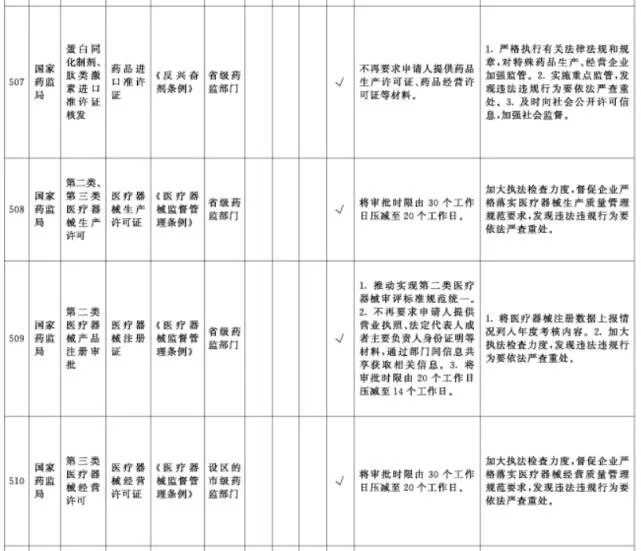
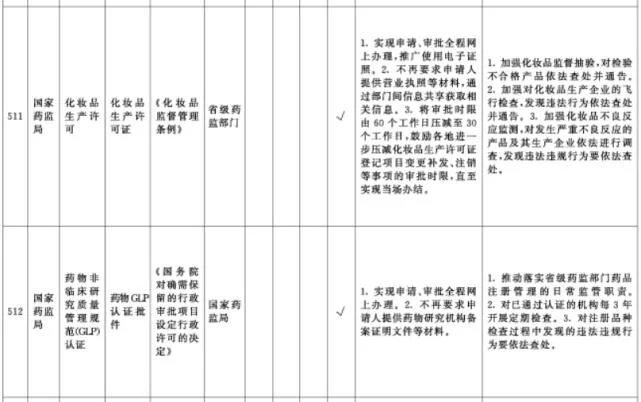
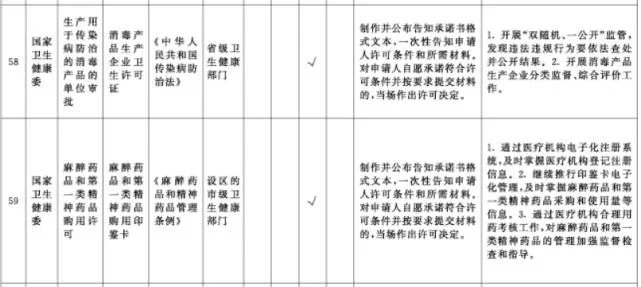
附件1.中央层面设定的涉企经营许可事项改革清单(2021年全国版)中涉及卫健、药监部门的改革项目共51项

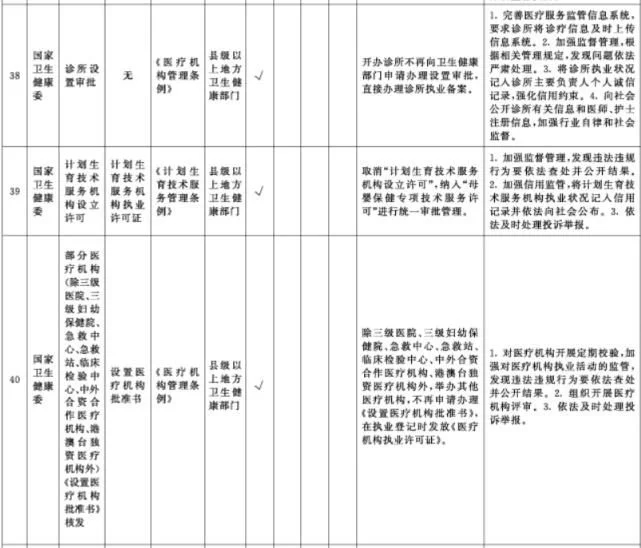
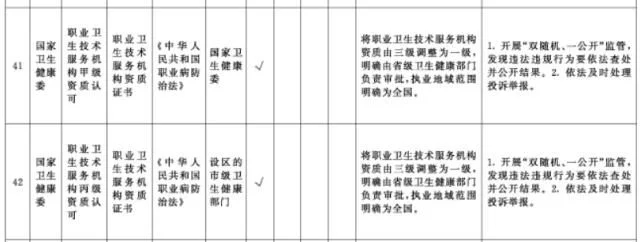

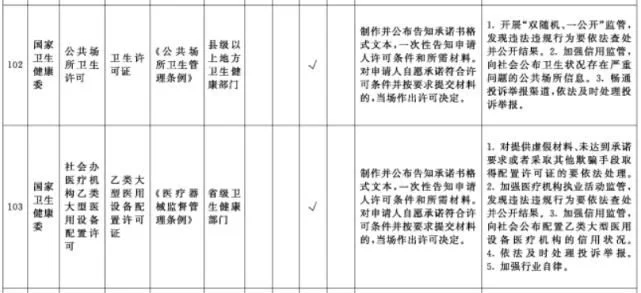
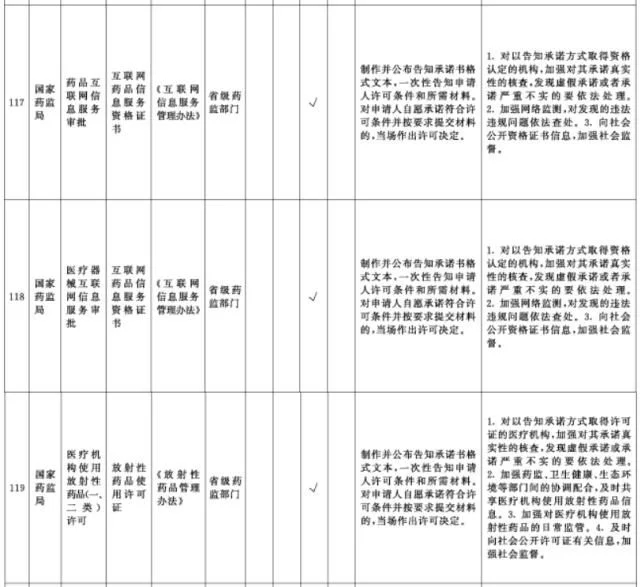




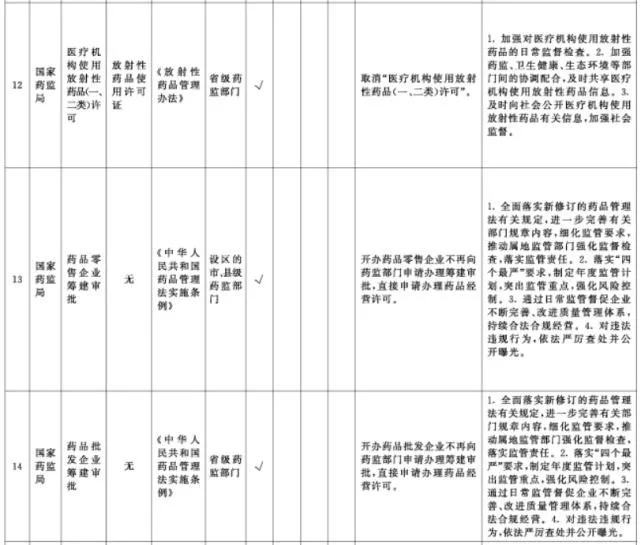
附件2. 中央层面设定的涉企经营许可事项改革清单(2021年自由贸易试验区版)中涉及卫健、药监部门的改革项目共10项

附件3. 国务院决定在自由贸易试验区暂时调整适用行政法规有关规定目录中涉及卫健、药监部门的改革项目共6项

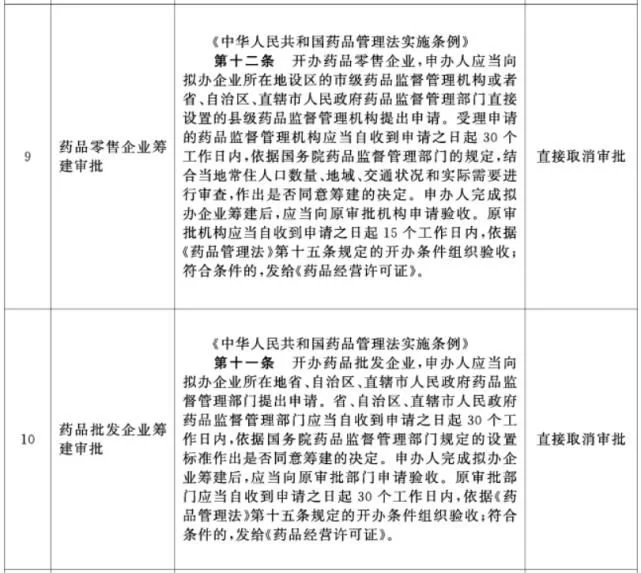

文章来源:国务院办公厅,看医界,筑医台资讯整理。





 >
>







